Botë
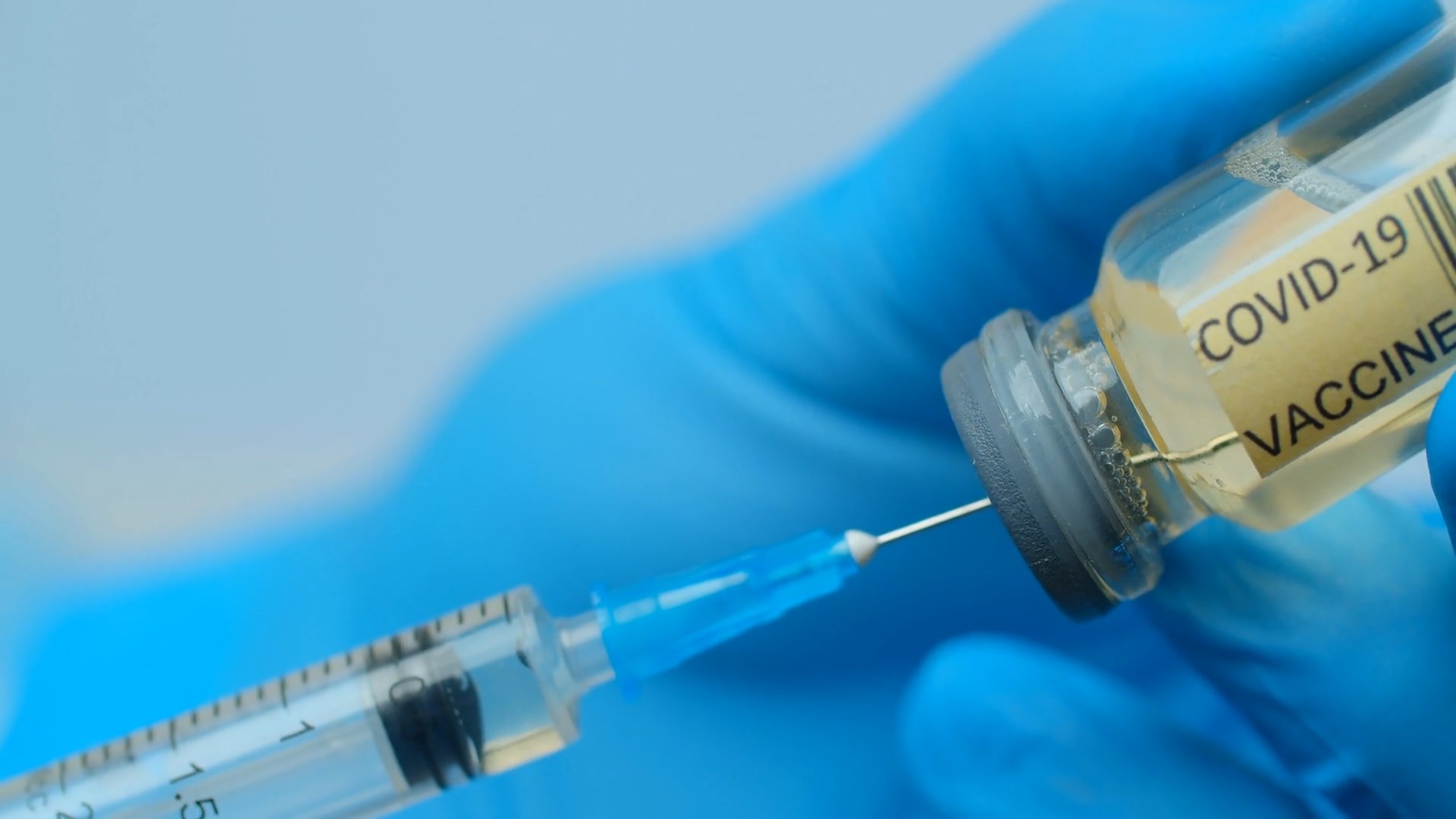
Vaksina e “Modernës” kundër COVID-19 në treg më 21 Dhjetor
-

 Ferizaj3 days ago
Ferizaj3 days agoNga reshjet e shiut sërish përmbytet segmenti i magjistrales Ferizaj – Prishtinë afër fshatit Muhoc
-

 Kosovë1 week ago
Kosovë1 week agoVrasjen e mbrëmshme në Prishtinë dyshohet se e bënë dy persona të maskuar
-

 Ferizaj14 hours ago
Ferizaj14 hours agoArrestohen edhe dy persona për vjedhjen në Dremjak të Ferizajt
-

 Ferizaj2 days ago
Ferizaj2 days agoProkuroria në Ferizaj do të mbajë konferencë për media për rastin e vrasjes të Muhamed Likës
-

 Ferizaj1 week ago
Ferizaj1 week agoArrestohet në Ferizaj i dyshuari për dhunim të një gruaje
-

 Arbëri3 days ago
Arbëri3 days agoNë Tiranë arrestohen dy shtetas të Kosovës, dyshohen për trafikim të armëve
-

 Ferizaj1 week ago
Ferizaj1 week agoNjë muaj paraburgim të dyshuarit për dhunimin e së miturës në Ferizaj
-

 Kosovë2 days ago
Kosovë2 days agoArrestohen 12 aktivistë në protestën kundër shtrenjtimit të rrymës
-

 Kosovë6 days ago
Kosovë6 days agoPresidenca kundërshton shtrenjtimin e rrymës
-

 Kosovë3 days ago
Kosovë3 days agoSeanca konstituive e Kuvendit të Kosovës më 15 prill
-

 Kosovë1 week ago
Kosovë1 week agoMinistri Damka akuzohet për “sulm” dhe “kanosje”